骨肉瘤转化研究新进展: 精科团队首次证实骨肉瘤新治疗靶点GPC3
缺乏药物作用靶点是骨肉瘤靶向治疗的“瓶颈”问题。精科生物李宏教授团队与广东省人民医院张余教授团队合作,在探寻骨肉瘤可靠治疗靶点方面取得进展,题为Frequently Expressed Glypican-3 As A Promising Novel Therapeutic Target for Osteosar-comas的阶段性研究成果近期在 Cancer Science (https://doi.org/10.1111/cas.15521)上发表。该研究发现,作为肝细胞癌免疫治疗靶点的GPC3在骨肉瘤中高频率表达(73.78%;45/61)且与CD133的共表达率为97.8%;抗GPC3 抗体通过阻断Wnt-β-catenin信号转导和诱导凋亡有效抑制GPC3阳性病例类器官(PDO)和异种移植瘤(PDX)的生长。这提示,针对GPC3的免疫治疗有望成为骨肉瘤个体化治疗的新途径,因此具有明显的转化肿瘤学意义。团队建立的骨肉瘤类器官和PDX模型为后续的临床前免疫治疗研究提供理想的离体和动物体内实验平台。

研究背景
骨肉瘤(OS)是最常见的骨源性恶性肿瘤,其治疗以手术为主,化疗为辅,但因其增殖迅速,容易复发,故预后不佳。对于一线化疗耐药骨肉瘤患者,目前还无有效的治疗靶标。本课题组的前期研究发现,1例多药耐药骨肉瘤存在Glypican-3 (GPC3) 突变和上调表达,抗 GPC3 免疫治疗可以有效抑制其类器官的生长。本研究的目的是进一步阐明GPC3 突变和表达在骨肉瘤中的普遍性及其治疗学意义。
研究方法
研究团队首先收集骨肉瘤患者穿刺及手术切除后的新鲜OS标本,在经过实验室处理后进行类器官培养并生成表达GPC3的骨肉瘤PDX。比对来源样本与类器官和PDX的一致性,并对OS的类器官和PDX应用抗GPC3抗体治疗,探究GPC3-Ab的作用机制。
研究结果
01
24例骨肉瘤患者的原发灶穿刺及手术样本成功培养成类器官
02
骨肉瘤类器官高度保留原代肿瘤组织形态学特点以及SOX9、Vimentin、CD133、GPC3等生物标记物的表达特征
03
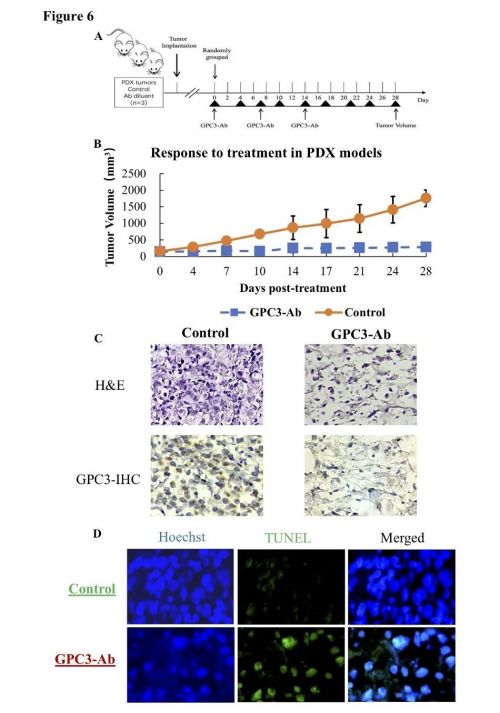
GPC3在骨肉瘤中高频率表达(73.78%;45/61),药敏检测结果显示,GPC3-Ab 能明显抑制GPC3高表达骨肉瘤类器官和PDX生长
04
骨肉瘤组织中同时表达GPC3和CD133,统计学分析表示,GPC3表达与肿瘤干细胞标记物CD133呈高度正相关(共表达率为97.8%;44/45)
05
GPC3-Ab 通过抑制Wnt-β-catenin通路活化以抑制骨肉瘤的生长
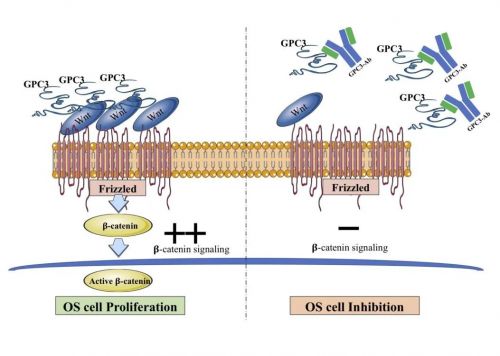
研究结论
本研究首次证明了GPC3-Ab 在GPC3阳性OS模型中的治疗有效性。为骨肉瘤治疗,尤其是针对GPC3和 CD133高频率共表达的骨肉瘤治疗提供了一个有前景的新型治疗靶点。
研究团队
李宏教授带领的类器官技术团队在PDO(人源肿瘤类器官)和PDX模型(人源肿瘤异种移植模型)方向研究应用经验丰富。首席科学家李宏教授曾成功研发全球首个高转移人胃癌PDX模型,获得卫生部科技进步奖。团队在骨肿瘤类器官研究领域深耕,目前全球已发表的骨肿瘤类器官文献仅有数篇,其中两篇由精科团队发表;GPC3与骨肉瘤关系的研究均为本团队报道。精科医学PDO技术成熟,建模成功率高达95%以上,配备完善的实验平台可满足PDO培养、肿瘤分子病理学、细胞分子生物学的多种临床科研需求。

?李教授实验中
广州精科医学检验所有限公司
广州精科医学检验所有限公司是精科生物集团旗下的全资子公司,是一家以类器官技术+基因组学技术为双驱核心的第三方医学检验所。公司在类器官方向致力于推动类器官技术的转化与应用,在科研上打造全面的类器官技术服务体系,而在临床上提供高效的类器官+NGS的综合检测服务。

?精科类器官培养实验室

